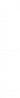IV.4 Les composés oxygénés
IV.4.1 Les alcools \(\left( {R - OH} \right)\) (les alcanols)
• Un alcool est caractérisé par la présence d'un groupement hydroxyle (\( - OH\)) lié à un atome de carbone tétravalent (R-OH).
Groupe principal : Suffixe = « ol »
• Le nom de l’alcool dérive de celui de l’alcane correspondant en remplaçant la terminaison « ane » par « ol ».
• L’atome de carbone portant le groupement (\( - OH\)) doit avoir l’indice le plus faible.
Il existe trois classes d’alcool :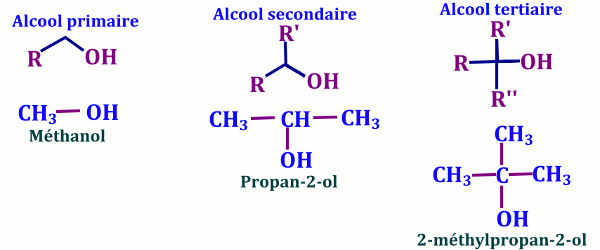
Les polyols sont des alcools possédant plusieurs groupes hydroxyles portés par des atomes de carbones tétragonaux différents.
a) Les diols
Ils ont deux fonctions alcool, le plus simple des diols est l’ethan-1,2-diol de formule brute \(HO - C{H_2} - \) \(C{H_2} - OH\)
b) Les triols
Ce sont des alcools possédant trois fonctions alcool dont le plus simple est le propan-1,2,3-triol de formule \(HO - C{H_2} - \) \(C{H_2}OH - C{H_2}\) \( - OH\)
IV.4.2 Les Ethers \(R - O - R'\) (Les alkoxyalcanes)
La déshydratation intermoléculaire au cours de la laquelle il y’a élimination d’une molécule d’eau entre deux molécules d’alcool conduit à la formation d’un éther-oxyde.
a) Les éthers linaires et ramifiés
Ils sont considérés comme des dérivés des alcools dans lesquels le proton hydroxylique du \( - OH\) est remplacé par un groupe alkyle \( - R'\).
Les éthers ne sont pas un groupe prioritaire et ils sont toujours désignés par le préfixe : oxy-
• La chaîne la plus longue est le groupe principal R ;
• Le radical restant, \( - R'\), est dérivé de l’alcool correspondant.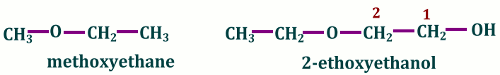
b) Ethers cycliques
Ils sont nommés avec le préfixe « oxa- » qui indique qu’un carbone du cycle a été remplacé par un oxygène et la nomenclature des cycloalcanes.
IV.4.3 Les aldéhydes \(R - CHO\)
Les aldéhydes sont des composés carbonylés dont l’atome de carbone du groupe carbonyle est lié à un atome d’hydrogène.
Le nom d’un aldéhyde s’obtient en remplaçant le « e » final du nom de l’alcane dont il dérive par le suffixe « al ».
Le groupe carbonyle des aldéhydes est toujours située en bout de chaîne, il est donc inutile de préciser la position du carbone fonctionnel.
La position des éventuels des substituants est aussi précisée en numérotant la chaîne carbonée la plus longue à partir du carbone fonctionnel du groupe aldéhyde.
• Un aldéhyde porte un groupement carbonyle (\(C = O\)) ou bout de la chaîne carbonée.
Le carbone du groupe \(CHO\) porte toujours le numéro 1.
• Le suffixe « -al » est utilisé lorsque le \(C\) du groupe aldéhyde fait partie du groupe de base (chaîne ou cycle principal) ;
• Le suffixe « -carbaldéhyde » est utilisé lorsque le \(C\) du groupe aldéhyde ne fait pas partie du groupe de base.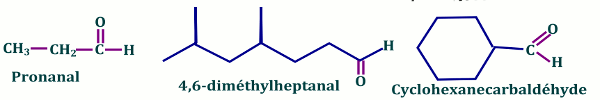
IV.4.4 Les cétones \(R - CO - R'\)
La cétone est un composé carbonylé dont l’atome de carbone du groupe carbonyle est lié à deux atomes de carbone tétragonaux.
Le nom d’une cétone s’obtient en remplaçant le « e » final du nom de l’alcane dont il dérive par le suffixe « one » précédé d’un indice précisant la position du carbone fonctionnel dans la chaîne carbonée principale. La chaine principale ( la plus longue) est numérotée de façon à attribuer au carbone fonctionnel le plus petit indice possible.
Une cétone porte un groupement carbonyle (\(C = O\)).
L'atome C du groupe carbonyle est lié à deux groupes alkyles (\(R - CO - R'\)).
Le groupe principal a pour suffixe « -one » 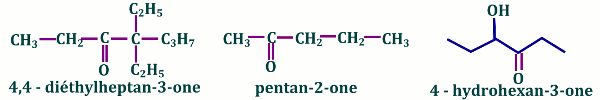 Si le groupe secondaire contient le groupe (\(C = O\)) son nom sera précédé du préfixe « oxo- »
Si le groupe secondaire contient le groupe (\(C = O\)) son nom sera précédé du préfixe « oxo- »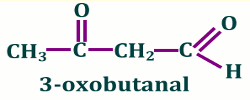
IV.4.5 Les acides carboxyliques RCOOH (acides alcanoïques)
Les acides carboxyliques sont des composés organiques dont la molécule présente le groupe fonctionnel –COOH appelé groupe carboxyle
La fonction carboxyle est prioritaire vis-à-vis de tous les groupes fonctionnels.
Les monoacide carboxyliques sont des acides qui contiennent un seul groupe carboxyle –COOH.
Pour les acides à chaîne linéaire, le nom s’obtient en remplaçant le « e » final de l’hydrocarbure correspondant par la terminaison « oïque », puis en faisant précéder le nom obtenu par le mot « acide »
La fonction carboxyle est prioritaire vis-à-vis de tous les groupes fonctionnels.
Groupe principal : Suffixe = acide ...-oïque
Les acides cycliques saturés sont nommés en tant qu'acides cyclo – alcane - carboxyliques.
Groupe principal : acide ... carboxylique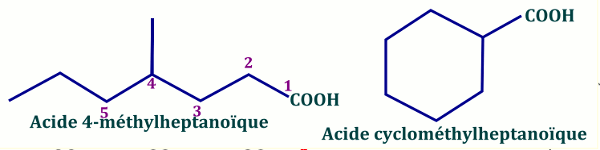 NB : Si le groupe secondaire a une fonction alcool, on a le préfixe « hydrohy- »
NB : Si le groupe secondaire a une fonction alcool, on a le préfixe « hydrohy- »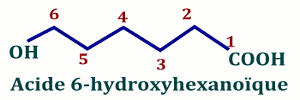 Si le groupe secondaire a une fonction aldéhyde, on a le préfixe « formyl »
Si le groupe secondaire a une fonction aldéhyde, on a le préfixe « formyl » Le carbone du groupement -COOH porte toujours le numéro 1.
Le carbone du groupement -COOH porte toujours le numéro 1.
• Pour les dérives alcènes, le principe de nomenclature est le même que précédemment, avec en plus l’indication de la position de la double liaison
Les polyacides contiennent au moins deux groupes carboxyle \( - COOH\)
• Pour les diacides saturés, la chaine principale est celle qui contient les deux carbones fonctionnels. Le sens de numérotation est celui qui accorde le plus petit indices aux substituants.
Le nom de l’acide s’obtient en remplaçant le « e » final de l’alcane correspondant par la terminaison « edioïques » 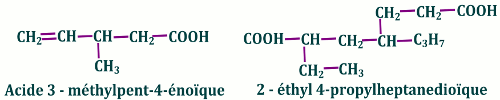 • Pour les diacides aromatiques, le nom s’obtient en ajoutant le suffixe « dicarboxylique » au nom de l’hydrocarbure correspondant, précédé du mot « acide »
• Pour les diacides aromatiques, le nom s’obtient en ajoutant le suffixe « dicarboxylique » au nom de l’hydrocarbure correspondant, précédé du mot « acide »
Dans ce cas, les carbones fonctionnels ne sont pas pris en compte dans la numérotation. Celle-ci commence par le carbone directement liée au premier groupe hydroxyle –COOH de sorte que l’atome C lié au second groupe hydroxyle porte le plus petit indice possible 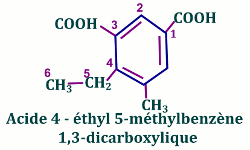
IV.4.5 Les esters \(R - CO - OR'\) de formule brute \({C_n}{H_{2n}}{O_2}\)
Un ester résulte de la réaction de la réaction entre un alcool et un acide carboxylique.
Le nom de l’ester s’obtient à partir de celui de l’acide carboxylique correspondant, en remplaçant la terminaison «oïques» par « oate », puis en ajoutant la préposition « de », suivie de nom du radical alkyle \(R’\). 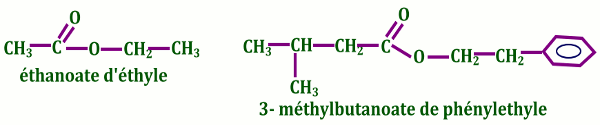
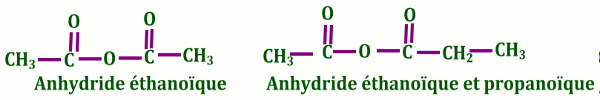
IV.4.6 Anhydrides d’acides \(RCOOOCR’\) de formule brute \({C_n}{H_{2n - 2}}{O_3}\)
Un anhydride d'acide résulte de la déshydratation intermoléculaire des deux molécules d’acide carboxylique.
Pour nommer un anhydride d’acide, on fait suivre le mot anhydride du nom de l’acide dont il dérive.
Lorsque les chaines carbonées de l’anhydride sont différentes (anhydride mixte), le nom dérive de ceux des acides correspondants.