Objectif :
- Donner la représentation spatiale d’une molécule.
1. Définition.
La stéréochimie est l’étude de la disposition spatiale des atomes constituants des molécules et des ions.
Lorsque deux ou plusieurs molécules diffèrent soit par leurs formules développées plane, soit par la disposition de leurs atomes dans l’espace, on dit que l’on a affaire à des isomères.
Il existe deux types d’isoméries : L’isomérie de constitution et l’isomérie de conformation.
1.2 L’isomérie de constitution.
On appelle isomères de constitution toutes les molécules qui ont la même formule brute, mais dont les atomes sont enchainés de manière différente tout en respectant la valence de chaque élément.
Il existe trois types d’isoméries de constitution :
1.2.1 L’isomérie de chaine.
Les isomères de chaine possèdent la même fonction chimique mais différent par l’enchainement des atomes de carbones les constituant.
Exemple : A la formule brute \({C_4}{H_{10}}O\), on peut avoir comme isomères de chaines
\({H_3}C - \) \(CH(C{H_3})\) \( - C{H_2}\) \( - OH\)
\({H_3}C - \) \(C{H_2} - \) \(C{H_2} - \) \(C{H_2} - \) \(OH\)
1.2.2 L’isomérie de position.
Les isomères de position possèdent la même chaine carbonée, la même fonction chimique, mais diffèrent par la position du groupe fonctionnel sur la chaine ou par la position de la liaison caractéristique.
Exemple : \({C_4}{H_{10}}O\)
\({H_3}C - \) \(C{H_2} - \) \(C{H_2} - \) \(C{H_2} - \) \(OH\)
\({H_3}C - \) \(C{H_2} - \) \(CH(OH)\) \( - C{H_3}\)
Exemple 2 \({C_4}{H_8}\)
\({H_2}C = \) \(CH - \) \(C{H_2}C{H_3}\)
\({H_3}C - \) \(CH = \) \(CH - \) \(C{H_3}\)
1.2.3 l’isomérie de fonction.
Les isoméries de fonctions diffèrent par la nature du groupe fonctionnel.
Exemple :
\({H_3}C - \) \(C{H_2} - \) \(OH\) et \({H_3}C - \) \(O - C{H_3}\)
2. La stéréo-isomérie.
Très souvent, les isomères on la même formule développée plane, mais diffèrent par leur structure spatiale, On parle dans ce cas de stéréo-isomérie. Il en existe deux types : La stéréo-isomérie de configuration et de conformation.
2.1 La stéréo-isomérie de conformation.
On appelle conformation d’une molécule les différentes structures spatiales qu’elle peut prendre par suite de la rotation autour de ses liaisons simples \(C - C\). Ses molécules sont appelées stéréo-isomères de conformation ou conformères.
La stéréo-isomérie de conformation se rencontre généralement chez les alcanes et les cyclanes.
Exemple :
La molécule d’éthane \({C_2}{H_6}\) possède deux types de conformations :
Le conformère E et le conformère D sont des stéréo-isomères de conformation.
- La conformation éclipsée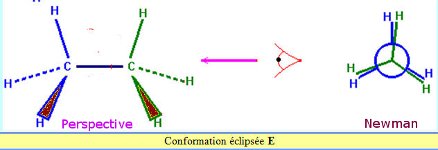 - La conformation décalée.
- La conformation décalée.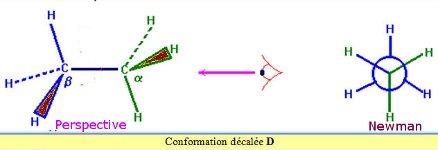 La conformation décalée est la plus stable car elle minimise l’encombrement stérique.
La conformation décalée est la plus stable car elle minimise l’encombrement stérique.
La molécule de cyclohexane possède également deux conformères stables (la conformation chaise et la conformation bateau).
Remarque :
Il est impossible d’isoler un conformère de l’autre. Ils existent tous à un moment donné dans un échantillon mais, avec des proportions dominantes des conformères les plus stables.
2.2 Stéréo-isomérie de configuration.
Deux cas de stéréo-isoméries de configuration se présentent :
- Soit la conformation est liée à une double liaison présente dans la molécule, on parle dans ce cas de diastéréo-isomères.
- Soit elle est liée à un atome de carbone asymétrique, on parle dans ce cas d’énantiomérie.
2.2.1 La diastéréo-isomère ou isomérie Z/E.
La présence d’une double liaison (CC) dans une molécule la rend rigide au niveau de cette liaison car il n’y a pas possibilité de rotation. Cette isomérie ce rencontre dans les composés éthyléniques de formule générale.
\(R'CH\) \( = CHR\)
R’ et R étant différents des atomes d’hydrogènes.
Dans le cas ou les groupements R et R’ sont du même coté de la double liaison, on parle d’isomérie Z et dans le cas contraire on parle d’isomérie E.
Ces deux isomères de configurations sont appelés diastéréo-isomères.
Exemple :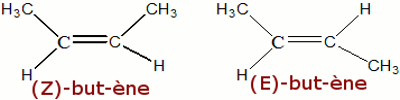 Remarque :
Remarque :
- Le passage d’un diastéréo-isomère à l’autre nécessite la rupture de la double liaison.
- Les diastéréo-isomères ont le même enchainement d’atome, la même formule
Semi-développée, mais des configurations spatiales et formules développées différentes. Ils ont donc des propriétés chimiques et physiques différentes.
2.2.2 L’énantiomère.
a) Le carbone asymétrique.
Un atome de carbone tétraédrique lié à 4 atomes ou groupe d’atomes différents est un atome de carbone asymétrique noté C*.
Exemple :
\(\begin{array}{*{20}{c}}{}&H&{}\\{}&|&{}\\{{H_3}C - }&{C*}&{ - COOH}\\{}&|&{}\\{}&{N{H_2}}&{}\end{array}\)
b) La chiralité.
Un objet tel une molécule ou un ion est chirale lorsqu’il n’est pas superposable à son image dans un miroir. Exemple : La main, le pied.
Une molécule chirale est capable de dévier le plan d’une lumière polarisée, cette molécule est dite optiquement active :
- Si la déviation de la lumière se fait à droite, la molécule est dite dextrogyre ou (+)
- Si la déviation se fait vers la gauche, la molécule est dite lévogyre ou (-).
Remarque :
- Une molécule ou un ion ne possédant qu’un seul atome de carbone asymétrique est toujours chirale.
- Dans le cas ou elle possède plusieurs atomes de carbone asymétrique, elle peut être achirale. Si en plus la molécule possède un plan de symétrie, elle est achirale, dans le cas ou elle n’en possède pas, elle est chirale.
- Une molécule chirale peut ne pas posséder de carbone asymétrique (exemple des allèles, de spiranes).
c) L’énantiomère.
Deux molécules images l’une de l’autre dans un miroir plan non superposable sont appelées énantiomères. A toute formule plane comportant un atome de carbone asymétrique correspond un couple d’énantiomère.
Un mélange équimolaire de deux énantiomères est un mélange racémique.
Exemple : La molécule ci-dessous possède deux énantiomères :
\(\begin{array}{*{20}{c}}{}&H&{}\\{}&|&{}\\{{C_2}{H_5} - }&{C*}&{ - COOH}\\{}&|&{}\\{}&{N{H_2}}&{}\end{array}\)
3. La représentation de Fischer.
La représentation de Fischer est très commode pour certaines molécules tel que les acides \(\alpha \)-aminés. Elle nécessite certaines règles :
- La chaine carbonée la plus longue est verticale.
- En groupement \({ - COOH}\) est en haut et le groupement –R en bas, tous les deux orientés vers l’arrière.
- Les groupements latéraux sont orientés vers l’avant.
Dans le cas des acides \(\alpha \)-aminés, si le groupement amino (\({ - N{H_2}}\)) est à droite, l’acide sera noté D, dans le cas ou il est à gauche il sera noté L.
Exemple :
Soit la molécule :
\(\begin{array}{*{20}{c}}{}&H&{}\\{}&|&{}\\{{H_3}C - }&{C*}&{ - COOH}\\{}&|&{}\\{}&{N{H_2}}&{}\end{array}\)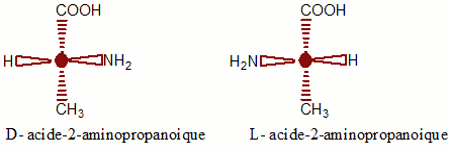 Remarque :
Remarque :
- Tous les acides α-aminés naturelles sont de la série L
- Les nomenclatures L et D n’ont rien avoir avec les termes dextrogyres et lévogyres.