Partie A : Évaluation des ressources / 24 Points
Exercice 1 : Vérification des savoirs / 8points
1) Définir les termes suivants : (0,5pt x2= 1pt)
a) Polymérisation ;
b) Couple oxydant-réducteur.
2) Choisir la réponse juste parmi celles proposées. (0,5pt x2 = 1pt)
a) Le carbone fonctionnel des alcools est :
i) Trigonal ;
ii) Tétravalent ;
iii)Tétragonal.
b) L’hydratation des alcènes conduit à :
i) Un alcool ;
ii) une cétone ;
iii) un aldéhyde.
3) Représenter le groupe fonctionnel des aldéhydes et des cétones. (1pt)
4) On considère l’équation-bilan suivante :
\({I_2} + 2{S_2}O_3^{2 - }\) \( \to 2{I^ - } + {S_4}O_6^{2 - }\)
5) Dire s’il s’agit d’une réaction d’oxydoréduction. Si oui préciser l’oxydant et le réducteur. (1,5pt)
6) Nommer les composés A ; B et C de formules semi-développées ci- dessous. (0,5pt x 3 =1,5pt)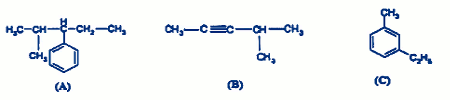 7) Donner deux méthodes de protection du fer contre la corrosion. (1pt x 2 = 2pt)
7) Donner deux méthodes de protection du fer contre la corrosion. (1pt x 2 = 2pt)
Exercice 2 : Applications des savoirs / 8points
1) On donne les potentiels standards suivants \({E^o}(P{b^{2 + }}/Pb)\) \( = - 0,13V\) et \({E^o}(C{u^{2 + }}/Cu)\) \( = 0,34V\).
a) Dire s’il se déroule une réaction chimique ou non lorsqu’on introduit une lame de cuivre dans une solution de sulfate de plomb. (1pt)
b) On réalise une pile à partir des deux couples ci-dessus :
i) Indiquer le pôle positif et le pôle négatif de cette pile. (1pt)
ii) Écrire l’équation- bilan de la réaction de fonctionnement de cette pile. (1,5pt)
iii) Calculer sa f.é.m. E. (1,5pt)
2) Le 1,2-difluoroéthylène \((FHC = CFH)\) peut être polymérisé.
a) Écrire son équation de polymérisation. (1pt)
b) Représenter le motif du polymère.(0,5pt)
c) Déterminer le degré de polymérisation, la masse molaire du polymère vaut 84,992kg/mol (1,5pt)
On donne masses molaires atomiques en g/mol : F=19 ; C= 12 ; H= 1.
Exercice 3 : Utilisation des savoirs / 8 points
1) Utiliser les nombres d’oxydation pour équilibrer l’équation ci-dessous : (1,5pt)
\({H_2}S{O_4} + C \to \) \(C{O_2} + S{O_2} + \) \(2{H_2}O\)
2) On veut vérifier la concentration \(Cr\) d'une solution aqueuse A de dioxyde de soufre \(\left( {S{O_2}} \right)\). A cet effet, on fait tomber goutte à goutte dans 20 cm3 de A, une solution de permanganate de potassium de concentration Co = 0,10mol/L.
a) Écrire l’équation-bilan équilibrée du dosage. Les couples en présence sont : \(SO_4^{2 - }/S{O_2}\); \(\left( {Mn{O^ - }/M{n^{2 + }}} \right)\). (1pt)
b) Il a fallu verser 12 cm3 de solution de permanganate pour atteindre l'équivalence, déterminer Cr. (1,5pt)
3) On considère un hydrocarbure B de densité de vapeur d= 3,655 dont on veut étudier la structure et les propriétés chimiques. La combustion complète d’une masse m = 0,875 ? de l’hydrocarbure ? produit m′ = 2,91 ? de dioxyde de carbone.
a) Déterminer la composition centésimale massique de l’hydrocarbure ?. (1pt)
b) En déduire la formule brute de ? et préciser à quelle famille de composé il appartient. (1,5pt).
c)Écrire les formules semi-développées possibles et les nommer. (1,5pt)
Partie B : Évaluation des compétences (16points)
Grand-père BAKO depuis deux semaines est souffrant, accompagné de son petit-fils KAMDEM, ils sont allés ce matin voir le médecin de famille pour vérifier sa glycémie (quantité de glucose contenue dans le sang) à jeun. Le médecin a prélevé 12mL de son sang auquel il a associé une quantité convenable de liqueur de Fehling en excès et à chaud. KAMDEM son petit-fils dit qu'il a observé que la liqueur de Fehling de couleur bleue foncée a donné avec son sang après un certain temps un précipité rouge- brique.
On met à votre disposition les documents ci-dessous.
Document1.
Le glucose \((C{H_2}(OH) - \) \(CH(OH) - \) \(CH(OH) - \) \(CH(OH) - \) \(CH(OH) - CHO)\) sera considéré comme un aldéhyde de formule générale \(R - CHO\).
Sa réaction avec la liqueur de Fehling se déroule de la manière suivante :
NB : Les equations ci-dessous sont reversibles.
\(2C{u^{2 + }} + 2O{H^ - } + \) \(2{e^ - } \to C{u_2}O\) \( + {H_2}O\) (1)
\(R - CHO + \) \(O{H^ - } \to R - \) \(CO{O^ - } + 2{H_2}O\) \( + 2{e^ - }\) (2)
\(2C{u^{2 + }} + 5O{H^ - }\) \( + R - CHO \to \) \(R - CO{O^ - } + \) \(3{H_2}O + C{u_2}O\)
(3) représente l'équation -bilan globale de cette réaction. Le précipité rouge -brique est le monoxyde de cuivre \(I(C{u_2}O)\). Une personne est atteinte de diabète si dans son sang la concentration massique en glucose est supérieure ou égale à 180mg/L.
Document 2. La concentration massique ou titre, est la masse en gramme de soluté dissoute dans un litre de solvant on a : \(C = \frac{m}{V}\) et s’exprime en g/L.
Le glucose: formule brute \({C_6}{H_{12}}{O_6}\); masse molaire moléculaire 180g/mol. Masse molaire moléculaire de l'oxyde de cuivre \(I(C{u_2}O)\) 144 g/mol.
Les résultats de la réaction entre les 12mL de sang de grand-père BAKO et la liqueur de fehling montrent la formation de 6mg de précipité rouge-brique de \(C{u_2}O\).
En t'appuyant sur tes connaissances et l'exploitation des informations ci-dessus,
1. Propose un protocole expérimental permettant de réaliser la réaction (3) 6 pts
2. Prononce toi sur l'état de santé de grand- père BAKO souffre-t-il de diabète ? 10 pts